J ADV RES│青岛农大王芹志与吴薇团队:生牛乳中的耐药基因组、细菌组与移动基因组特征解析
- 2026-04-16 08:36:48


集约化养殖作为全球乳制品生产的主导模式,集约化动物养殖与常规性抗微生物药物预防用药,加剧了抗菌剂耐药性(AMR)风险。然而,抗生素耐药基因在区域性集约化奶牛养殖系统中的时空传播模式仍未得到充分阐明。本研究通过表征不同样本基质中的抗生素耐药基因,阐明区域性集约化奶牛养殖系统中抗生素耐药基因的时空传播模式。本研究采用了一种综合性的研究方法,将宏基因组测序与全面的实验验证(细菌分离、抗菌药物敏感性试验、基于PCR的ARGs检测、生物膜形成测定以及接合实验)相结合,以表征从中国山东省42家集约化养殖场收集的539份样本(包括原料奶、饲料、水和乳房拭子)中的抗生素耐药基因组。结果显示DY地区样本表现出最显著的微生物多样性(16347个物种)和最高的ARG丰度(547个亚型),其中主要为β-内酰胺酶基因(56.3%)。多重耐药决定因子在所有样本类型中普遍存在。肺炎克雷伯菌被确定为高风险载体,对β-内酰胺类抗生素的耐药率达96.43%,其多重耐药率为25%。关键的是,接合实验证实了blaSHV基因可水平转移至大肠杆菌,表明其具有跨物种传播潜力。此外,研究者还发现生物膜形成与增强的β-内酰胺耐药性之间存在显著相关性(P < 0.05),这表明生物膜在维持耐药性方面起着作用。
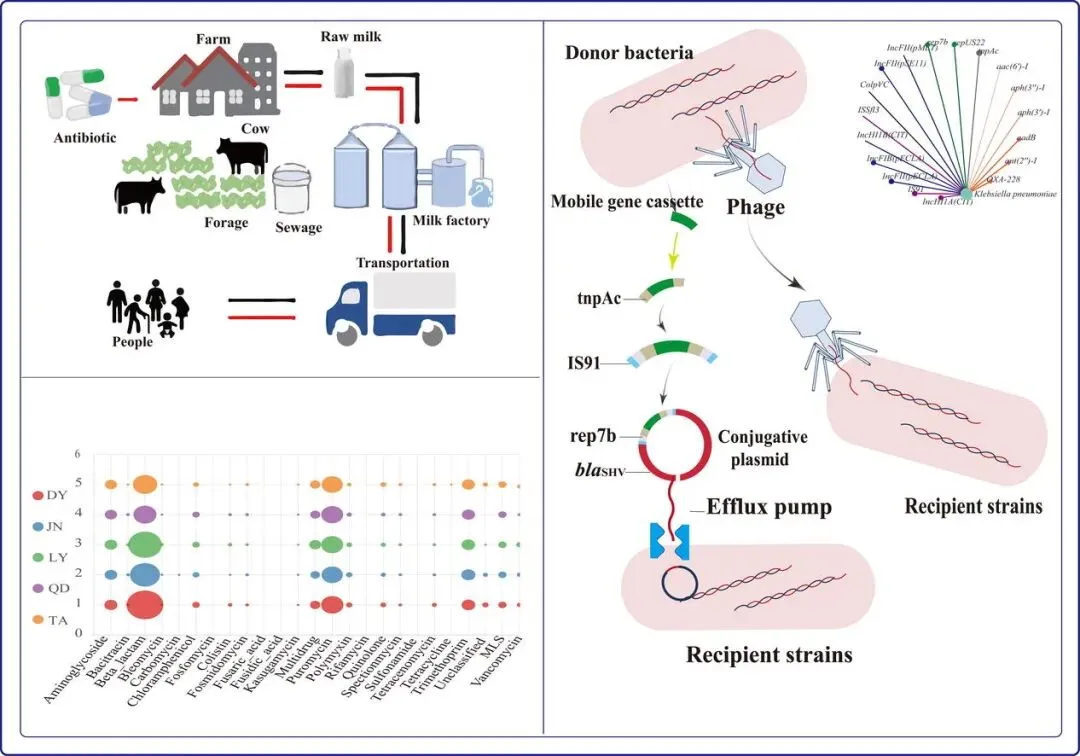
图片摘要
论文ID
原名:Metagenomic characterization of the resistome, bacteriome and mobilome in raw milk from intensive farming systems
译名:基集约化养殖系统生牛乳中的耐药基因组、细菌组与移动基因组的宏基因组学特征解析
期刊:Journal of Advanced Research
IF:13
发表时间:2025.11
通讯作者:王芹志,吴薇
通讯作者单位:青岛农业大学食品科学与工程学院
实验设计

结果
1.产业链中微生物的迁移驱动了抗生素耐药基因传播的高风险
研究者从山东省5个地区(DY、QD、LY、JN、TA)的生牛乳样本中,分离出大肠杆菌、肺炎克雷伯菌、沙门氏菌、志贺氏菌和乳房链球菌5种菌株,其中前4种均属于肠杆菌科(图3a)。研究者选取宏基因组测序结果中丰度排名前100的致病菌进行分析,结果显示:DY地区的致病菌累积丰度最高(图1a),且致病菌α多样性(辛普森指数,图1b)最高;基于主坐标分析(PCoA)的β多样性结果显示,DY地区与其他地区的距离相对较远(图1c),表明其菌群结构存在显著分化,这与DY地区多样性最高的分析结果一致。相比之下,QD地区的物种丰度和α多样性均最低。研究者对生牛乳中抗生素耐药基因(ARG)的分析表明:QD地区的耐药基因亚型数量最少(250种),而DY地区的耐药基因多样性明显更高(396种亚型),总丰度占5个地区总检测量的72.3%,其中β-内酰胺酶基因占主导地位(308种亚型,占比56.3%)(图2c)。Upset图分析显示,DY地区的特有耐药基因亚型数量在5个地区中最多(70种),QD地区最少(20种)(图2a)。其中,β-内酰胺类耐药基因在不同地区和不同样本间存在显著差异。因此,可以得出结论:微生物物种多样性与抗生素耐药基因多样性呈正相关。

图1 不同地区生牛乳中细菌物种的丰度与多样性。(a)所有生牛乳样本中丰度排名前20的细菌物种丰度分析;(b)辛普森指数箱线图;(c)样本间微生物群落结构的主坐标分析(PCoA)。
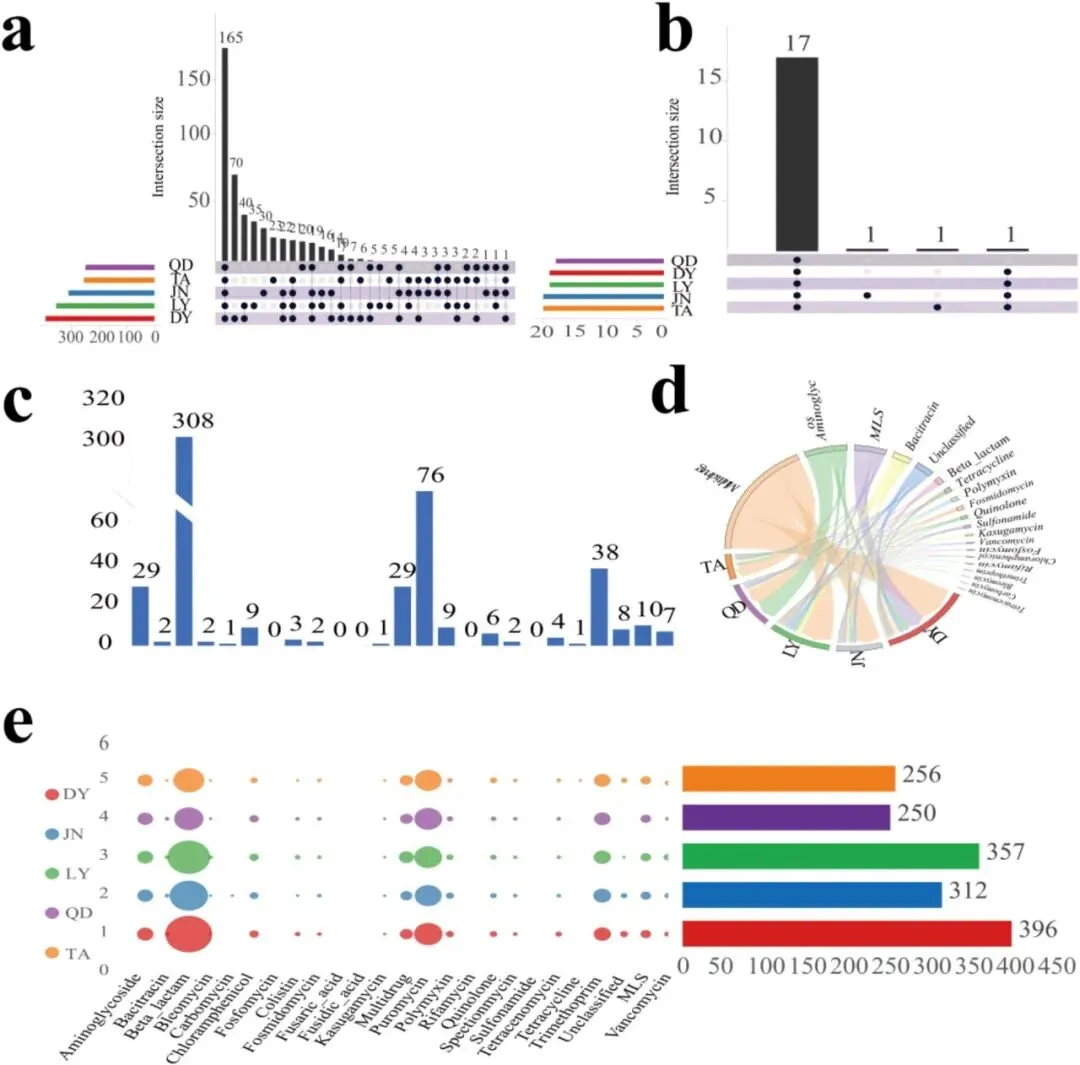
图2 不同地区耐药类型及耐药基因统计。(a)和(b)通过R软件(v4.2.0)的UpSetR包绘制,分别以弦图和Upset图展示不同地区耐药类型与耐药基因的共有特征及特有特征;上方柱状图表示交集大小(共有耐药类型数量),下方点阵图及左侧柱状图显示各地区对这些交集的贡献度;(c)柱状图呈现20种主要抗生素耐药类型的分布情况,其中柱高对应相应耐药表型/基因型的数量;(d)通过R软件(v4.2.0)的circlize包绘制,弦图展示抗生素耐药类型与地区分布的关联特征,突出耐药性传播的潜在关联及相关地区;(e)展示20种耐药类型在不同地区的分布情况,数据通过Excel进行统计分析。耐药基因(ARG)亚型包含所有检测样本中丰度非零的可检测亚型;组合点阵图(左)与柱状图(右)呈现抗生素耐药表型的地区分布:点阵图显示5个地区耐药性的存在情况及发生频率,柱状图汇总各地区耐药相关标志物的总数量。
研究者对生牛乳中丰度排名前20的致病菌分析显示,35%的物种属于肠杆菌科,为绝对优势菌科(图3a)。研究者对这7个物种的溯源结果表明,除来源未知的物种外,大肠杆菌、肺炎克雷伯菌和肠炎沙门氏菌是溯源频率最高的物种;其中,大肠杆菌和肺炎克雷伯菌也通过实验以较高丰度分离出来。此外,尽管肺炎克雷伯菌在临床领域已得到广泛研究,但其在食品生产链中的风险尚未得到充分探讨,因此本研究对肺炎克雷伯菌开展了进一步分析。研究发现,水体是这些致病菌的主要来源,57.7%的致病菌来源于水体(图3b),而来自乳房拭子的比例最低。据此推测,这些细菌可从水体(生活用水和牛饮用水)、饲料、乳房拭子等环境样本迁移至牛奶中,导致生牛乳中致病菌丰度较高;这些物种携带的耐药基因可能随之传播,形成跨区域抗生素耐药基因(ARG)传播的高风险“细菌-基因共迁移”模式。
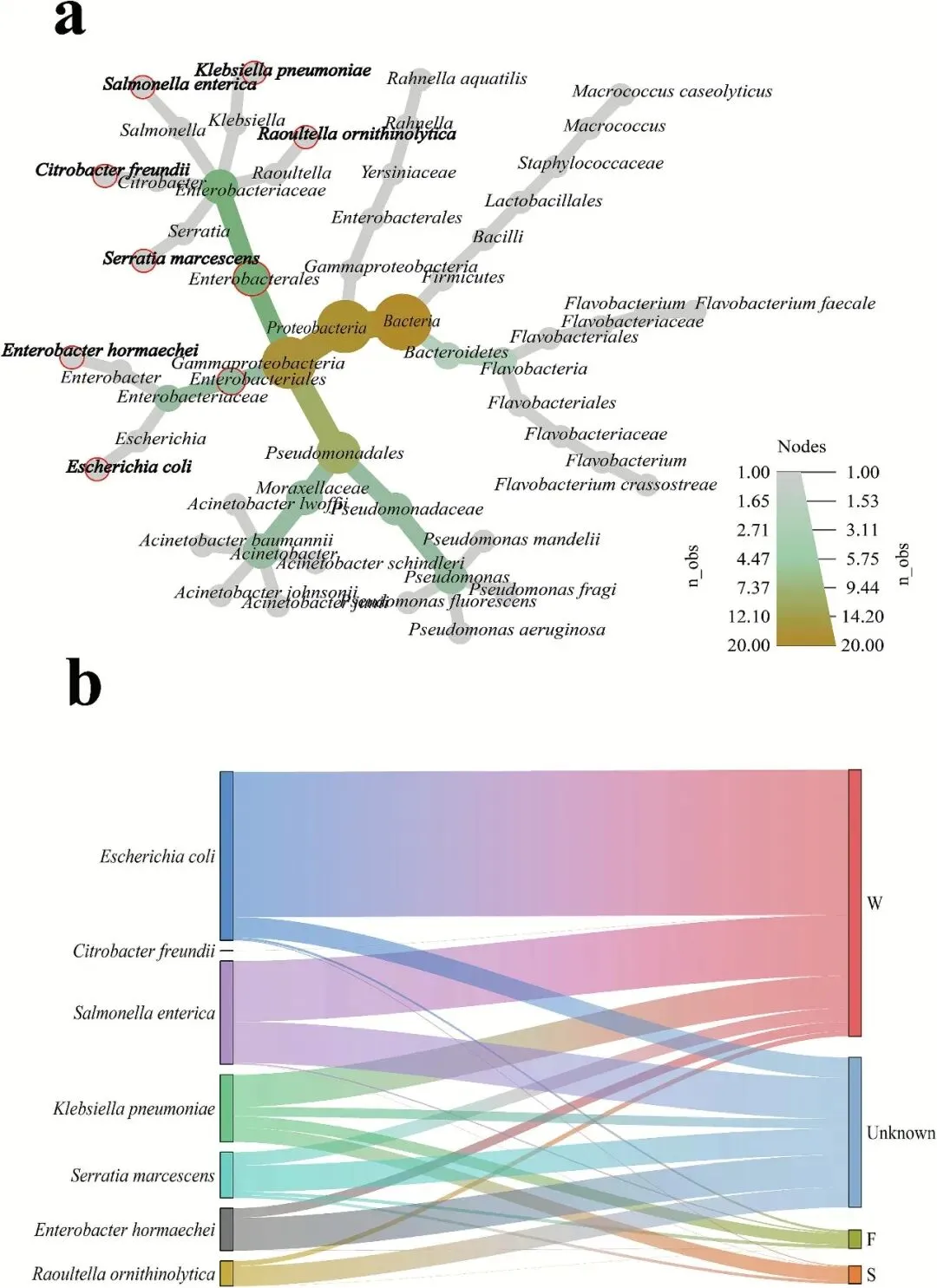
图3 丰度排名前20的细菌物种溯源分析。(a)丰度前20的细菌类群在不同分类水平间的相关性分析;(b)不同细菌物种的来源环境溯源结果,该分析通过R软件(v4.2.0)的SourceTracker包与FEAST包计算完成。其中,W:水体;F:饲料;S:乳房拭子。
2.肺炎克雷伯菌:多重抗生素耐药表型与基因型的协同进化
肺炎克雷伯菌占生牛乳分离致病菌的49.1%(图4b),不同地区的分离株数量存在显著差异(图4a)。该菌在QD和DY地区的检出率最高(均为25.00%),其次是LY地区(21.43%)。本研究针对肺炎克雷伯菌,选取7大类共9种抗生素进行抗菌药物敏感性试验(AST),包括:β-内酰胺类[氨苄西林(AMP)、青霉素(PEN)、美罗培南(MEM,碳青霉烯类)、头孢他啶(CAZ)、头孢曲松(CTR)、头孢噻肟(CTX)]、喹诺酮类[恩诺沙星(ENR)、环丙沙星(CIP)],四环素类[四环素(TET)],氨基糖苷类[庆大霉素(GEN)],氯霉素类[氟苯尼考(FLO)],多粘菌素类[多粘菌素B(PB)],磺胺类[磺胺甲噁唑(SXT)]。耐药基因检测结果显示,除四环素、庆大霉素和恩诺沙星外,肺炎克雷伯菌分离株对其余所有测试抗生素的耐药率均高于大肠杆菌,其中对β-内酰胺类抗生素的耐药性最强。具体而言,对氨苄西林的耐药率高达96.43%(27/28),25%(7/28)的分离株为多重耐药菌(MDR),显著高于大肠杆菌[4.55%(1/22)]。基因分型结果表明,耐药性由gyrA(100%)、blaSHV(82.14%)、sul1(50%)和blaCTX-M(46.43%)等关键基因驱动,且大多数耐药基因的检出率均高于大肠杆菌。此外,46.43%的肺炎克雷伯菌分离株具有中高强度的生物膜形成能力,且生物膜强度与对氨苄西林和青霉素的耐药性呈显著正相关(P< 0.05)(图4c)。
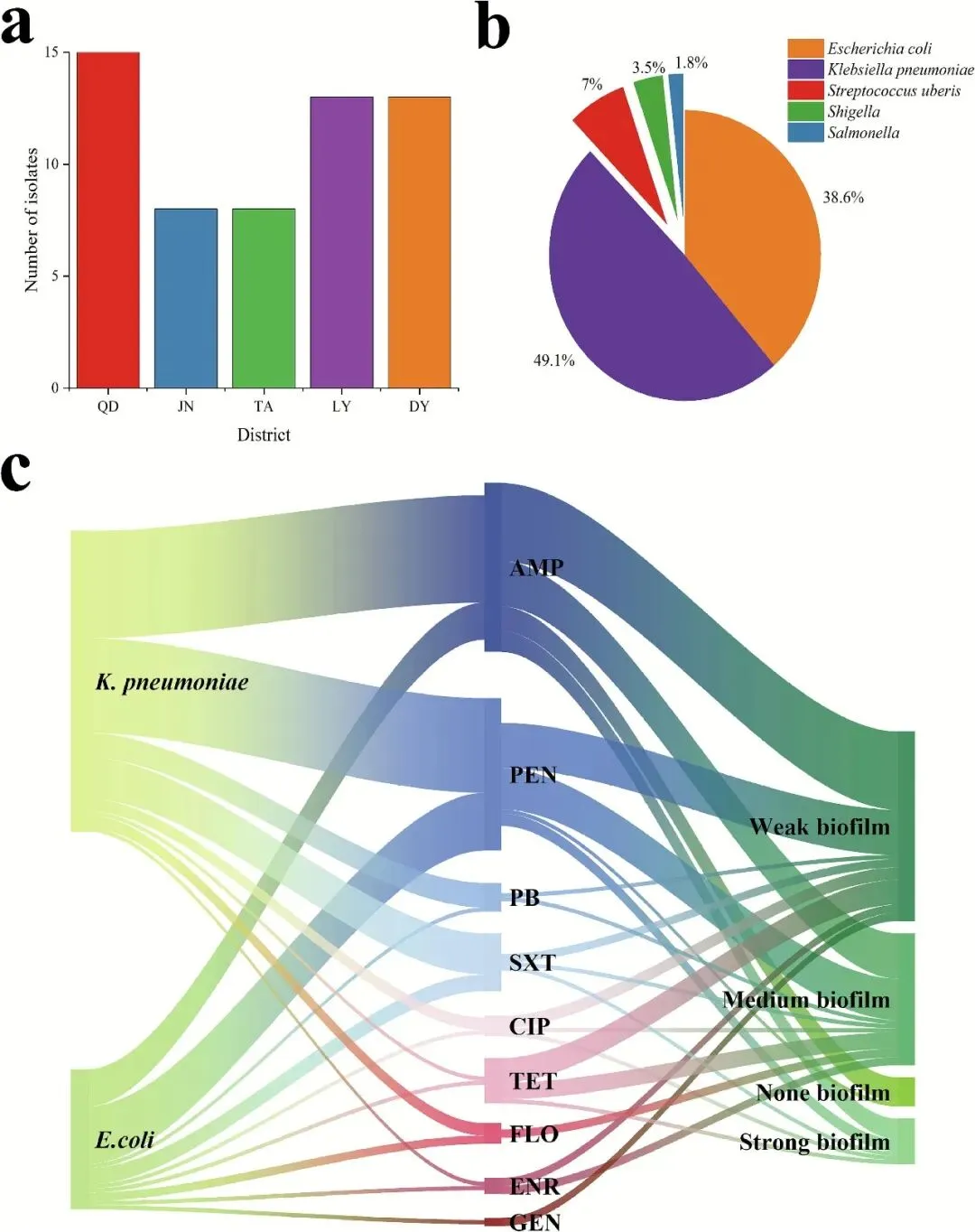
图4 致病菌分离与生物膜分析。(a)山东省不同地区样本的细菌分离数量;(b)各细菌在分离菌株中的检出率;(c)肺炎克雷伯菌与大肠杆菌分离株的生物膜与抗生素耐药性相关性分析。
3.可移动遗传元件介导的blaSHV基因跨物种转移机制
接合实验证实,肺炎克雷伯菌K01菌株可将blaSHV基因转移至同种细菌(转移频率:3.3×10-5)和大肠杆菌E02菌株(8.6×10-6),实现跨属传播,但向金黄色葡萄球菌的转移效率显著更低(6.1×10-6)(图5a)。值得注意的是,供体菌和受体菌均为肺炎克雷伯菌时转移频率最高,而受体菌为金黄色葡萄球菌时转移频率最低,这清晰地表明接合效率存在种间差异(图5a)。后续基因组DNA分析显示,大多数接合子菌株中均存在blaSHV耐药基因(图5b),但部分接合子中该基因缺失,提示基因转移成功率存在变异性。本研究对获得的12株接合子菌株进行最低抑菌浓度(MIC)测定,结果显示:与受体菌相比,所有接合子菌株的氨苄西林(AMP)浓度均升高,且均对氨苄西林产生耐药性。肺炎克雷伯菌与可移动遗传元件(MGEs)的相关性分析显示,插入序列(IS家族)和整合子(Int家族)的相关性最强。因此,研究者推测IS家族和整合子可能促进耐药基因的转移。
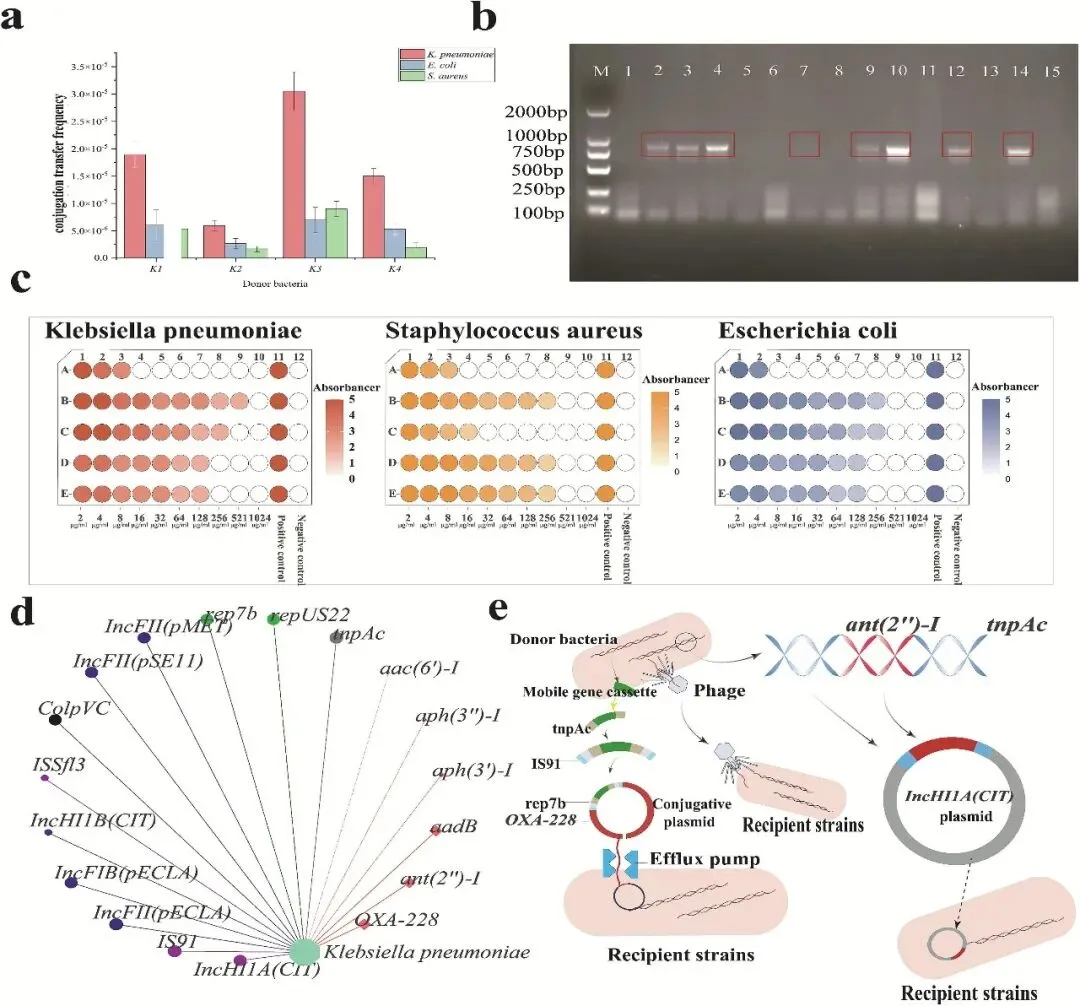
图5 接合实验。(a)接合转移频率;(b)耐药基因接合子验证。1-5:肺炎克雷伯菌(受体菌),k1、k2、k3、k4(接合子);6-10:大肠杆菌(受体菌),E1、E2、E3、E4(接合子);11-15:金黄色葡萄球菌(SA,受体菌),S1、S2、S3、S4(接合子);(c)接合子最低抑菌浓度实验。A行为受体菌,B、C、D、E行为接合子菌株,1-10列为氨苄西林(AMP)指数稀释液,浓度由低到高递增;(d)与肺炎克雷伯菌高度相关的丰度前100的抗生素耐药基因(ARGs)及可移动遗传元件分布分析;(e)接合作用与转导作用介导的抗生素耐药基因(ARG)转移示意图。
讨论
1.区域耐药性分化的生态与人为驱动机制
本研究发现,DY地区生牛乳中的抗生素耐药基因ARGs丰度(396种亚型)和微生物多样性显著高于QD等其他地区。这种地理差异可能源于多重驱动因素:DY位于黄河三角洲流域,该地区土壤中某些重金属的累积量时空变化较小。这些重金属可能激活微生物的应激反应通路(如omp基因),增加外膜通透性,并通过影响DNA转移与复制(如trfAp、traJ基因)间接促进抗生素耐药基因(ARG)的富集。此外,DY地区的集约化养殖模式以高饲养密度和常规性抗生素预防用药为特征,这可能产生强烈的选择压力,有利于抗生素耐药基因(ARG)的存续与传播。这一模式与全球其他高强度乳制品产区的研究结果一致。例如,美国的研究表明,使用抗生素的传统奶牛场,其粪便和牛奶中的抗生素耐药基因丰度和多样性显著高于有机牧场。同样,荷兰和新西兰的研究证实,含有抗生素的粪便用作肥料是抗生素耐药基因(ARG)向土壤和水体环境扩散的明确途径。相比之下,在抗生素监管更严格、饲养密度更低的欧洲地区(如部分斯堪的纳维亚国家),乳制品中的抗生素耐药基因(ARG)多样性相对较低,这凸显了养殖管理措施在塑造耐药组中的作用。同时,拟杆菌目物种中由可逆启动子调控的聚糖合成位点,是临床相关抗生素耐药基因(ARG)产生的重要热点区域,这进一步加剧了blaSHV等基因的传播(检出率:82.14%)。
2.肺炎克雷伯菌介导的耐药基因跨物种传播网络
生物膜也会影响抗生素耐药性的形成。这在乳制品生产场景中尤为重要,近期研究表明,肺炎克雷伯菌在乳制品加工设备表面具有较强的生物膜形成能力,这有助于其持续存活并成为耐药基因交换的热点区域。本研究发现,从牛奶中分离的肺炎克雷伯菌对β-内酰胺类抗生素的耐药率高达96.43%(27/28),且生物膜形成能力(46.43%的分离株具有中高强度生物膜)与blaSHV基因转移效率(向大肠杆菌的转移频率为2.1×10-5)呈显著相关性。生物膜通过物理屏障作用,使氨苄西林的最低抑菌浓度(MIC)值提高了64倍(4-256μg/mL),这一现象与Hall-Stoodley等人提出的通透性抑制机制一致。此外,生物膜内的胞外DNA可能为种间基因交换提供微生态位。
值得注意的是,大量研究表明,Inc型质粒和IS家族转座子在抗生素耐药基因(ARG)的传播中发挥关键作用。已有研究表明,辅助质粒IncFIB(Mar)在高毒力碳青霉烯耐药肺炎克雷伯菌(hv-CRKP)的进化中起关键作用,该质粒可将非接合型巨型毒力质粒高效转移至耐碳青霉烯肺炎克雷伯菌(CRKP),促进耐药基因和毒力基因的传播。
从传播途径来看,肠道作为微生物聚集和基因交换的重要场所,为抗生素耐药基因(ARG)的传播创造了有利条件。一项针对犊牛肠道中携带超广谱β-内酰胺酶(ESBL)的大肠杆菌的研究表明,肠道内细菌克隆与质粒之间存在复杂的相互作用,质粒可在不同细菌克隆间传播耐药基因。这意味着,即使只有0.001%-0.1%的乳制品相关肺炎克雷伯菌在巴氏杀菌后存活,这些残留菌株进入肠道后,仍可能利用肠道微生态环境,通过水平基因转移将IncFIB型质粒携带的耐药基因传播给其他肠道微生物。
此外,环境因素对抗生素耐药基因(ARG)传播的影响也不容忽视。研究表明,农药和生长促进剂等残留物的累积同样会加速微生物耐药性的传播。同时,生物膜可作为多重耐药(MDR)质粒的“避难所”,并促进质粒的水平转移,这对多重耐药性的传播具有重要意义。在乳制品生产环境中,若残留的肺炎克雷伯菌及相应耐药质粒在适宜条件下持续存在,可能发生类似的传播现象,增加环境微生物群中抗生素耐药基因(ARG)的传播风险。结合本研究中菌株的质粒特征,进一步提示在从生产到消费的整个乳制品产业链中,存在由肺炎克雷伯菌及其携带的IncFIB型质粒引发抗生素耐药基因(ARG)传播的潜在风险。
为阻断这一传播途径,未来研究可评估乳铁蛋白或基于CRISPR的靶向消毒技术用于乳制品行业的应用潜力。研究表明,肺炎克雷伯菌的内源性CRISPR-Cas3系统可在体外和体内高效清除耐药质粒,为应用CRISPR技术消除乳制品相关肺炎克雷伯菌的耐药质粒提供了理论基础。尽管CRISPR-Cas9介导的靶向技术在其他领域已展现出强大的基因编辑能力,但其在清除乳制品相关肺炎克雷伯菌抗生素耐药质粒中的效果仍需未来进一步探索。
3.乳制品产业链耐药性综合防控策略
基于发现的高风险区域抗生素耐药基因分布特征及肺炎克雷伯菌介导的基因转移机制,研究者提出以下防控框架,为全球乳制品抗菌剂物耐药性(AMR)管理提供科学参考。建议以宏基因组技术为核心工具,该技术可同时捕获547种抗生素耐药基因亚型和16347种微生物物种,灵敏度比传统培养方法高37%。丹麦综合抗微生物药物耐药性监测与研究计划(DANMAP)等项目的成功实施,证实了宏基因组技术用于大规模监测的可行性——该计划自启动以来,已为国家政策制定提供依据,并使畜牧业的抗生素使用量减少了40%以上。此外,该技术在农业“一体健康”框架中的应用日益广泛,研究表明其可有效追踪抗生素耐药基因(ARG)从牧场环境到食品产品的传播动态,验证了其在实际监测中的作用。本团队开发的两项检测技术可有效补充这一监测体系:一是基于荔枝状Ag@ZIF-8@Au等离子体纳米复合材料的表面增强拉曼散射SERS平台,可实现对可能驱动抗生素耐药基因选择的痕量污染物的高灵敏度检测;二是MXene/Auapt-Au@Ag NFs SERS生物传感器,可快速特异性定量检测牛奶中金黄色葡萄球菌等耐药致病菌。两者共同为乳制品抗菌剂耐药性防控提供了可现场应用的工具支持。结合地理信息系统(GIS)动态追踪高风险区域的抗生素耐药基因(ARG)热点,应优先在DY等抗生素耐药基因(ARG)富集区域开展试点试验,验证其成本效益。必须严格限制β-内酰胺类药物的预防用药,这一措施在欧盟等监管严格的地区已被证实有效。对于靶向干预,基于CRISPR的质粒清除技术是一种具有潜力但尚处于起步阶段的策略。针对肺炎克雷伯菌IncFIB质粒介导的blaSHV基因传播,可探索基于CRISPR-Cas9的靶向消毒技术——实验室可控条件下的研究显示,该技术的清除率较高(如体外实验中达93%)。但在实际应用前,需解决诸多显著局限性,包括大规模开发和递送CRISPR系统的高成本、对微生物群落的潜在破坏,以及CRISPR抗性质粒的快速进化。同时,可利用乳铁蛋白抑制生物膜形成,实验数据显示其可使生物膜强度降低高达52%,为挤奶设备和储奶罐的生物膜控制提供了一种更易即时应用的天然替代方案。建议将β-内酰胺类基因占比阈值纳入国家标准,参考欧盟法规EC No 853/2004抗生素优化管理,并引入区块链技术实现产业链透明可追溯。整合已验证政策(抗生素限制)、近成熟技术(宏基因组监测、乳铁蛋白)和探索性技术(CRISPR)的多维度策略,可能是一个最稳健的方案。该框架通过技术创新与政策协调,为全球乳制品行业提供了从源头到终端的抗菌剂耐药性防控路径。未来,需在奶牛场开展试点试验,验证这些技术的可扩展性,尤其要关注宏基因组监测的成本效益比、CRISPR或乳铁蛋白的递送机制,并利用流行病学模型量化抗生素耐药基因(ARG)通过乳制品传播对人类健康的风险。
版权声明
本文转载“微生态”,版权属于原作者所有,文章翻译和转载为学术传播。
团队水平有限,翻译和转载难免有不恰当之处,请批评指正,多多包涵!
往期精彩回顾:
